Признаки различия металлов и неметаллов.
Металлы в отличие от неметаллов имеют следующие характерные признаки:
- Внешний блеск
- Хорошую проводимость тепла и электрического тока
- Достаточно высокую прочность
- Хорошо куются и свариваются
- Кристаллическое строение тела
- Определенную температуру плавления и кристаллизации
Неметаллы (металлоиды) не имеют внешнего блеска, плохо проводят тепло и электрический ток, имеют сравнительно низкую прочность, не куются и не поддаются сварке. Они также не имеют кристаллического строения тел и определенной температуры плавления и кристаллизации.
Классификация металлов и сплавов.
Металлы и сплавы по ГОСТ 5200—50 классифицируют по:
- Числу компонентов
- Содержанию легирующих компонентов
- Степени чистоты
- Характеру компонентов
По числу компонентов металлы разделяют на простые металлы и металлические сплавы. Простым металлом называют металл, не содержащий в себе легирующих компонентов. Металлическим сплавом называют кристаллическое вещество, в составе которого имеется несколько металлов и металлоидов. Сплавы бывают двух-, трех- и более компонентными.
Компонентом называют химический элемент, входящий в состав металла или сплава. Компоненты подразделяют на основные и легирующие.
Основным называют такой компонент, который преобладает в металле или сплаве. Легирующим компонентом называют компонент, вводимый в состав сплава для получения необходимых требуемых технических свойств.
По содержанию легирующих компонентов сплавы делят на низколегированные, среднелегированные и высоколегированные. Низколегированным называют сплав, содержащий в своем составе легирующих компонентов менее 2,5%, среднелегированным — содержащий в своем составе легирующих компонентов 2,5— 10%. Сплав, содержащий в своем составе легирующих компонентов более 10%, называют высоколегированным.
По степени чистоты металлы и сплавы делят на пониженную, среднюю, повышенную, высокую и особую чистоту. Металлы и сплавы пониженной чистоты имеют степень чистоты 95—99%, средней чистоты — 99—99,9%, повышенной чистоты — 99,9—99,99%, высокой чистоты— 99,99—99,999%, а особой чистоты — 99,999—99,9999 %.
Области применения металлов и сплавов.
В зависимости от климатических условий, параметров работы той или иной конструкции (характера и величины нагрузки, давления, среды, рабочей температуры) применяют черные или цветные металлы. Углеродистые стали применяют для изготовления листовых и решетчатых конструкций, котлов, трубопроводов и корпусов различного рода машин.
Легированные стали применяют для изготовления ответственных конструкций, емкостей и трубопроводов, транспортирующих агрессивные и токсичные продукты. Чугун в основном применяют для изготовления больших тяжеловесных станин и трубопроводов (канализация, водопровод и т.д.); цветные металлы, например -сплавы алюминия и магния, — в тех отраслях промышленности, где наряду с высокой прочностью к конструкциям предъявляют требования высокой коррозионной стойкости и небольшого удельного веса.
Никель, медь, свинец и их сплавы применяют при сооружении металлургических, нефтеперерабатывающих и химических заводов.
Строение и кристаллизация металлов и сплавов.
Все вещества состоят из молекул, а молекулы из атомов. Атомы в свою очередь состоят из ядра и электронов, вращающихся вокруг него. Самым простым является атом водорода, состоящий из ядра и одного электрона. Атом железа состоит из ядра и 26 электронов.
Соединения атомов образуют различные вещества. Вещества по количеству находящихся в них химических элементов бывают простыми и сложными.
Простые вещества состоят из атомов одного химического элемента, а сложные — из нескольких химических элементов. К простым веществам относятся: чистое железо, чистая медь, чистый никель и т.д. К сложным веществам относятся сплавы (сталь, чугун, бронза, латунь и т.д.). Некоторые простые вещества имеют различное расположение атомов и в связи с этим различные свойства. Например: алмаз —очень твердое вещество, а графит— мягкое, однако и то и другое состоит из углерода.
Явление существования химического элемента в виде различных простых веществ называют аллотропией.
По внутреннему строению все твердые тела делят на две группы: аморфные и кристаллические.
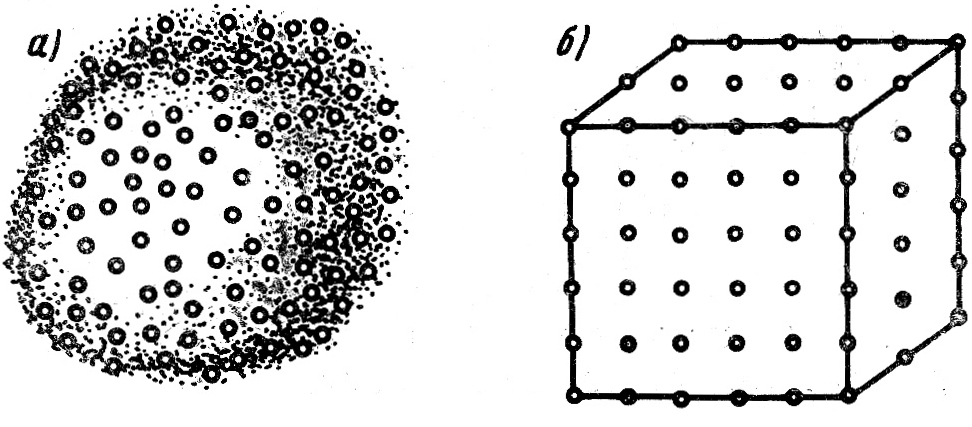
Аморфные —это такие тела, в которых атомы расположены беспорядочно (рис. 1 ,а). К ним относятся стекло, воск, смола, пластмасса и т.д. Аморфные тела имеют следующие особенности:
- при нагревании постепенно размягчаются и переходят в жидкое состояние, а при охлаждении постепенно затвердевают, т. е. они не имеют определенной точки плавления и кристаллизации
- свойства аморфных тел одинаковы, независимо от того, в каком направлении они подвергаются нагрузке.
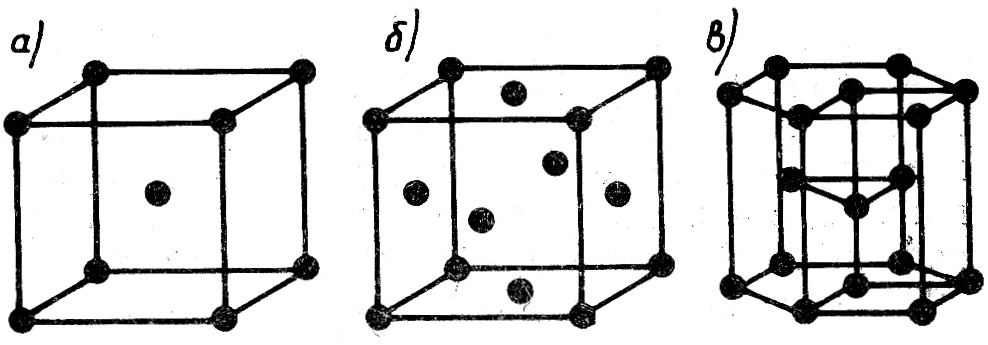
Кристаллические — это такие тела, атомы в которых расположены в правильном геометрическое порядке (рис. 1,6). Металлы, как правило, являются кристаллическими телами. При правильном геометрическом расположении атомов в кристаллическом теле можно выделить правильную объемную фигуру, называемую кристаллической решеткой. Примеры кристаллических решеток металлов показаны на рис. 2. На рис. 2,а показано расположение атомов в объемно-центрированном кубе, состоящем из 9 атомов, из которых 8 расположены в вершинах куба и 1 в центре на равном расстоянии от шести его граней.
Решетка, называемая кубом с центрированными гранями (рис. 2,6), состоит из 14 атомов, из которых 8 находятся в вершинах куба, а 6 расположены в центрах граней. Гексагональная решетка (рис. 2,б) состоит из 17 атомов, 12 из которых расположены в вершинах узлов верхнего и нижнего оснований шестигранной призмы, 2 — в центрах верхнего и нижнего оснований и 3—внутри призмы. Кристаллическая решетка объемно-центрированного куба характерна для железа (при температуре ниже 910°С), хрома, молибдена, вольфрама и других металлов; гранецентрированного куба— для железа (при темлературе выше 910°С), алюминия, меди и свинца. Гексагональную решетку имеют цинк, магний, титан и другие металлы.
Атомы элементов имеют весьма малые размеры. Для измерения размеров и расстояний между их центрами принята единица измерения ангстрем — Å. Один Å равен 0,00000001 см. Размеры атомов различных элементов находятся в пределах 1—5 Å, т. е. в 1 см размещаются десятки миллионов кристаллических решеток.
Тела, имеющие кристаллическое строение, обладают следующими характерными свойствами:
- они могут приобретать правильную внешнюю форму, соответствующую той или иной геометрической фигуре, которая получается благодаря определенному взаимному расположению атомов
- при разрушении тела кристаллического строения разделяются на части по определенным плоскостям, называемым плоскостями спайности или скольжения
- процесс перехода из твердого состояния в жидкое и обратно происходит при определенной температуре — точке плавления или затвердевания. Переход жидкого тела (металла) в твердое с образованием кристаллов называют кристаллизацией.
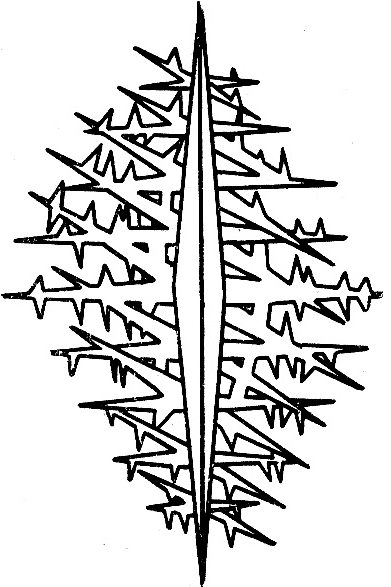
В процессе кристаллизации кристаллы часто принимают форму, напоминающую ветви дерева, откуда и возникло их название «дендриты» (греческое слово «дендрос» — дерево), рис. 3. При достаточном количестве частиц расплавленного металла промежутки между ветвями дендрита оказываются заполненными— в этом случае образуется зерно. Установлено, что на величину зерен оказывает значительное влияние число центров кристаллизации, а также скорость, с которой растут кристаллы вокруг образовавшихся центров. С увеличением количества центров кристаллизации увеличивается число зерен, а их размер уменьшается. Кристаллизация металла может быть первичной и вторичной.
Процесс перехода жидкого металла в твердое—кристаллическое состояние называют первичной кристаллизацией. Изменение в твердом состоянии внутреннего строения (структуры) металла после первичной кристаллизации называют вторичной кристаллизацией.
Для того чтобы увидеть зерна, их расположение и величину, из металла делают шлифы, которые подвергают травлению, т. е. смачивают их реактивом — жидкостью особого состава. Различные металлы травят разными реактивами. Внутреннее строение металла (шлифа), определенное простым глазом без увеличения или с небольшим увеличением с применением лупы, называют макроструктурой. Внутреннее строение металла, определенное при помощи микроскопа, называют микроструктурой.